Põhiline erinevus: neeldumine on massiline nähtus, milles absorbeerub täielikult tahke või vedela kehasse, moodustades ühendi või lahuse. Teisest küljest on adsorptsioon pinna nähtus, mille puhul adsorbaadi molekulid keskenduvad ainult adsorbendi pinnale.
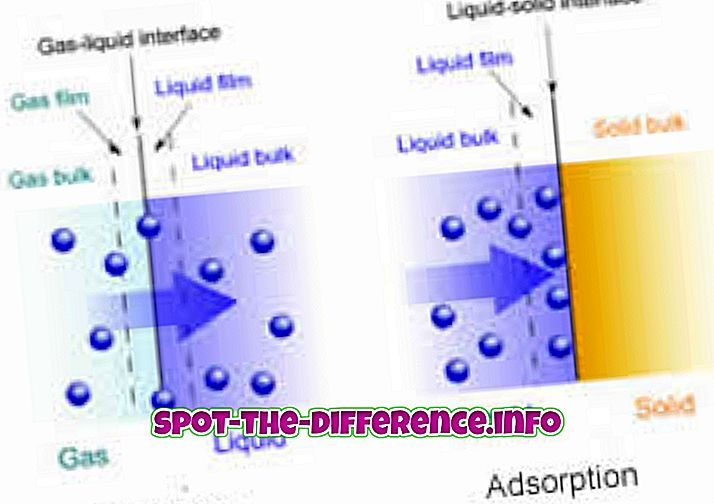
Keemiline reaktsioon - kaaliumkarbonaadi lahuses absorbeeritud süsinikdioksiid
Füüsiline protsess - Õhk imendub vees lahustamisega

On kahte tüüpi adsorptsioonirežiime - keemiline ja füüsiline. Keemilisel adsorptsioonil liidetakse molekulid ja pind nõrkade Vander'i seinte jõududega. Teiselt poolt, keemilise adsorptsiooni korral moodustub molekulide ja pinna vahel keemiline side.
Seetõttu on peamine erinevus adsorptsiooni ja imendumise vahel see, et imendumine on suurem nähtus, mis tähendab, et see juhtub kogu materjali kehas, samas kui adsorptsioon jääb pinna nähtuseks. Adsorptsioon on alati eksotermiline, samas kui absorptsioon on endotermiline. Sorptsioon hõlmab nii absorptsiooni kui adsorptsiooni protsesse.
Adsorptsiooni ja absorptsiooni võrdlus:
Adsorptsioon | Imendumine | |
Määratlus | Gaasi või vedeliku lahustumine tahke aine või vedeliku pinnal | Aine difusioon vedelasse või tahketesse ainetesse, et saada lahus või ühend |
Näide | Inertsed gaasid adsorbeeritakse süsi. | Kuiv käsn neelab vett |
Soojusvahetus | Eksotermiline, välja arvatud H2 adsorptsioon klaasile | Endotermiline |
Tasakaalu saavutamine | Võrreldes kiiremini | Võrreldes aeglaselt |
Kontsentratsioon | Kontsentratsioon adsorbendi pinnal erineb lahtiselt | Kontsentratsioon jääb kogu materjali ulatuses samaks |
Esinemissagedus | Algselt on see kiire, kuid hiljem hakkab see langema | See toimub ühtse määra alusel |