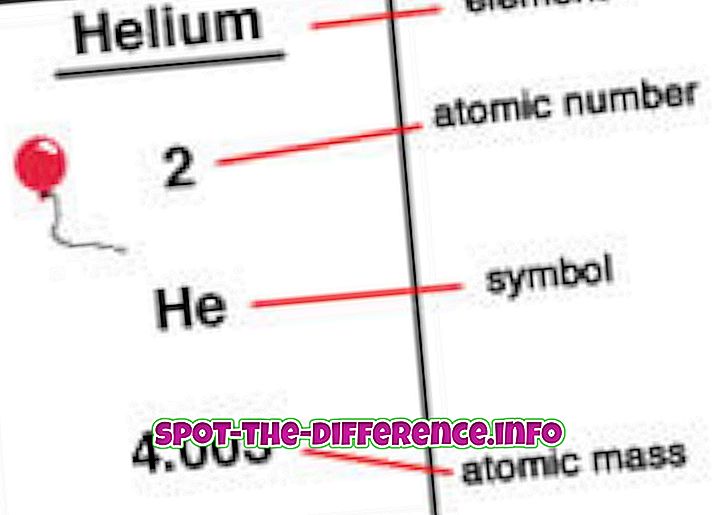
Põhiline erinevus: Aatomimass on lihtsalt konkreetse isotoobi mass või aatomi prootonite, neutronite ja elektronide kogumass. Aatomarv on elementide tuumas leiduvate prootonite arv.
Olgem ausad, et keemia on segane, erinevate elementide hulk, aatomnumbrid, sidemed, mass, kaal, aatomid jne. Kõik need sõnad hakkavad pärast teatud aja möödumist hägustuma, et inimene ei saa enam teistest eristada. Noh aatomimass ja aatomi number on kaks sellist sõna, mida sageli segi ajada ja kasutatakse vaheldumisi.
Aatomimass on aatomi mass, kui see on rahul. Seda seetõttu, et kui aatom liigub väga suure kiirusega, kipub see massi suurenema. Kuigi määratluse kohaselt on aatomimass kõigi prootonite, neutronite ja elektronide mass, on elektronid liiga väikesed, et tuumamassi oluliselt muuta. Enamikul perioodilise tabeli elementidest on isotoopid ja neutronite arvu erinevuse tõttu muutub ka iga isotoobi mass.
Aatomimassi väljendamiseks kasutatakse aatommassiühikuid või amu. Üks aatomimass on võrdne 1/12-ga süsinik-12 massist. Kui aatomi mass jagatakse süsinik-12 massi 1/12-ga, saadakse elemendi suhteline mass. Objekti suhteline mass on tegelikult elemendi aatommass, kuna see arvutatakse kõigi vaadeldavate isotoopide järgi. Seda ei tohiks aga pidada elemendi aatommassiks.

Aatomarv on elementide tuumas leiduvate prootonite arv. Kui aatom on neutraalne, tähendab see, et ta on sama palju prootoneid ja elektrone. Aatomnumbrit tähistatakse Z-ga. Kuna igal elemendil on erinev arv prootoneid, kasutatakse seda numbrit ka elemendi esindamiseks. Isotoopidel on tavaliselt sama aatomnumber, kuid klassifitseeritakse nende aatommassiga, näiteks Carbon-12, Carbon-13.
Elemendid paigutatakse perioodilisele tabelile aatomnumbri järjekorras. Aatomi number on elemendi vasakpoolses ülanurgas ülekirjutusena. Aatomnumbrid võivad aidata avaldada elementi puudutavat teavet ja paljud inimesed näevad aatomi numbrit ja näitavad, milline element see on. Samuti räägib see sellest, kus perioodilises tabelis seda saab ja kas see on vedelik, gaas või tahke. Aatomite arv annab teavet ka tuuma laadimise, oksüdeerumisolekute, sidumisomaduste, ioonide laadimise jne kohta.