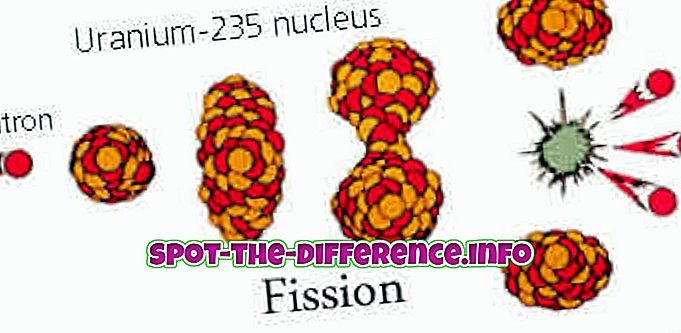
Oluline erinevus: sulamine on aine muutmine tahkest vedelikust. Seda tehakse tavaliselt aine kuumutamisega. Sulatamine on aga protsess, mille abil keemiline reaktsioon muudab aine või maagi puhtamaks.

Sulamine on aine muutmise või konverteerimise protsess tahkest kuni vedelaks vormiks. See on aine lihtne kuumutamise protsess sulamispunktini, kus aine hakkab veelduma. Paljudel juhtudel pannakse need sulatamiseks suure rõhu all ning kasutatakse ka soojuse ja rõhu kombinatsiooni. Kuumuse ja rõhu kombinatsiooniga võib aine sulatada ka madalamal temperatuuril. Sulamine toimub üldiselt selleks, et ainet või elementi vormida teatud kuju, nii et seda saaks kasutada mitmel viisil.
Sulamistemperatuur on temperatuur, kus tahkis hakkab muutuma oma vormi vedelikuks. Sulamistemperatuuril on tahke ja vedela vormi faas tasakaalus. See tähendab, et sulamistemperatuuril on aine tahke ja vedela vormi osa võrdne. Elemendi sulatamise protsessis muutub viskoossus ka vedelas olekus. Viskoossust võib nimetada vedeliku “paksuseks”. Näiteks on mee viskoossus suurem kui vees. Aine viskoossus muutub temperatuuri tõustes. Ained sulatatakse mitu korda teatud temperatuurini, et saavutada märkimisväärne viskoossus, nii et seda saab kasutada edasises protsessis.

Teisest küljest on sulatus metallide eraldamine maagidest, mis on kõige puhtamad. See protsess hõlmab kemikaale ja soojust maagi sulatamiseks ja selle puhastamiseks metallideks. Sulatamine toimub põhimetallide nagu raud, vask, hõbe ja kuld. Kemikaale, näiteks redutseerivaid aineid kasutatakse muude elementide pesemiseks maagist gaasideks või räbu (jäätmed); see jätab vaid metalli taga. Süsinik on kõige sagedamini kasutatav redutseerija. Metallide tootmisel on redutseerijana kaks kõige olulisemat vormi süsinikmonooksiid ja süsinikdioksiid. Enamik maagidest on ebapuhtad, mille jaoks puhastusvahendit, nagu lubjakivi, kasutatakse lisandite eemaldamiseks jäätmetena ja puhast metalli saamiseks. Sulatamine on väga tavaline ja oluline protsess, mida kasutatakse metallide puhta vormi saamiseks.