Peamine erinevus: Molaarsus, mida tuntakse ka molaarse kontsentratsioonina, mõõdab aine moolide arvu lahuse liitri kohta. Molaarsust tähistatakse pealinnaga M. Molality mõõdab aine lahustite arvu kilogrammi kohta. Molaarsust tähistatakse väiksema tähega m.
Mõlemad mõisted põhinevad arvutustel, mitu mooli on praeguses lahenduses. Lahust võib määratleda kui homogeenset segu, mis tähendab, et kahte või enamat komponenti on segatud selliselt, et seda ei saa palja silmaga eristada. Need kaks mõistet nõuavad moolide mõistmist, kuna see määrab lahuses olevate moolide arvu. Moolide teooria avastas Itaalia teadlane Amedeo Avogardo.
Aastal 1811 tegi Avogardo ettepaneku, et gaasi maht on antud temperatuuri ja rõhu juures proportsionaalne aatomite või molekulide arvuga, olenemata nende olemusest. Seda mõistet tuntakse Avogardo konstantsena. Seda defineeritakse kui koostisosade (tavaliselt aatomite või molekulide) arvu ühes moolis antud ainest. Maalilises mõttes esindaks üks mooli ainet elementis leiduvate aatomite ja molekulide arvu. Näiteks: hapniku aatommass on 16, mis esindaks ühe mooli hapniku massi. Niisiis, ühe mooli hapniku mass oleks 16 grammi. Avogardo sõnul oleks ühe mooli hapniku sama aatomite arv kui üks mool vesinik. Kuid need võivad erineda kaalu poolest.
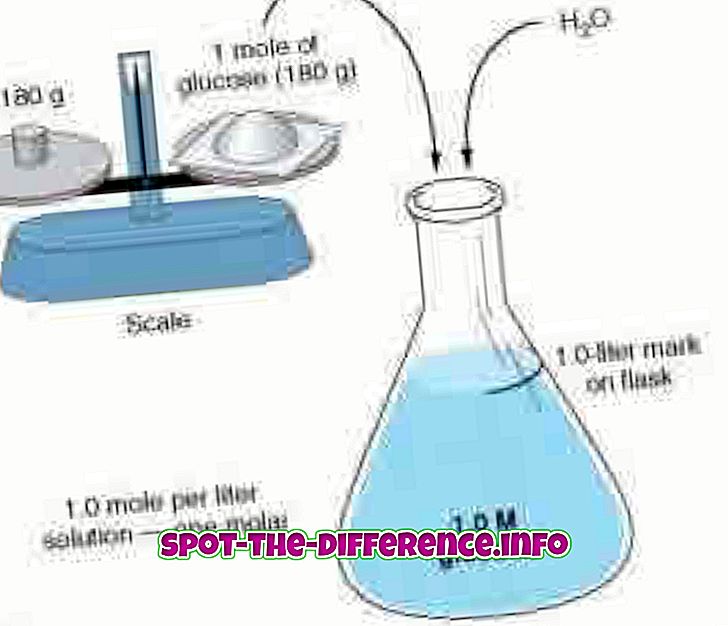
Molaarsus ja molaarsus mõõdavad kontsentratsiooni, kasutades kahte erinevat lähenemist. Molaarsus, mida tuntakse ka molaarse kontsentratsioonina, mõõdab aine moolide arvu lahuse liitri kohta. Molaarsust tähistatakse pealinnaga M. Nii et 1, 0M lahusega märgitakse, et see sisaldab 1 mooli lahustunud lahust liitri kohta. Näiteks: vee ja suhkru lahus. Kui lahust mõõdetakse 1, 0 M, siis lahusel on 1 mooli suhkrut ühe liitri lahuse kohta. Molaarsust tuntakse ka kui aine kontsentratsiooni, kontsentratsiooni, aine kontsentratsiooni või lihtsalt kontsentratsiooni. Molaarsust võib arvutada valemiga: M = mol (moolide arv) / L (lahuse maht liitrites).

Molaarsus mõõdab aine moolide arvu lahusti kilogrammi kohta. Molaarsust tähistatakse väiksema tähega m. Seega näitas 1, 0 m lahus, et see sisaldab 1 mooli soluuti kilogrammi lahusti kohta. Eristame soluuti lahustist. Lahusti on aine, mis lahustatakse mõnda teise ainesse. Lahusti on aine, mis lahustab lahustunud aine. Seega, kui vett ja suhkrut segatakse kokku, oleks suhkur lahustunud ja veega lahusti. Lahus oleks segatud suhkru vesi. Nüüd on molaalsuses äärmiselt oluline, et mutid jagataks lahusti massiga, mitte lahusega. Molaarsust võib arvutada valemiga: m = mol (moolide arv) / KG (lahusti mass kilogrammides).
Miks erinevus? Noh, mõlemat kasutatakse temperatuuri käsitlemisel. Kui lahus hakkab temperatuuri muutuma, kasutatakse molaarsust. Kuid lahenduste puhul, mis jäävad konstantse temperatuurini, kasutatakse molaarsust. Seda seetõttu, et temperatuuri tõustes või langedes muutub lahuse maht ja see mõjutab otseselt molaarsust. Seega kasutatakse kontsentratsiooni arvutamiseks molaarsust.