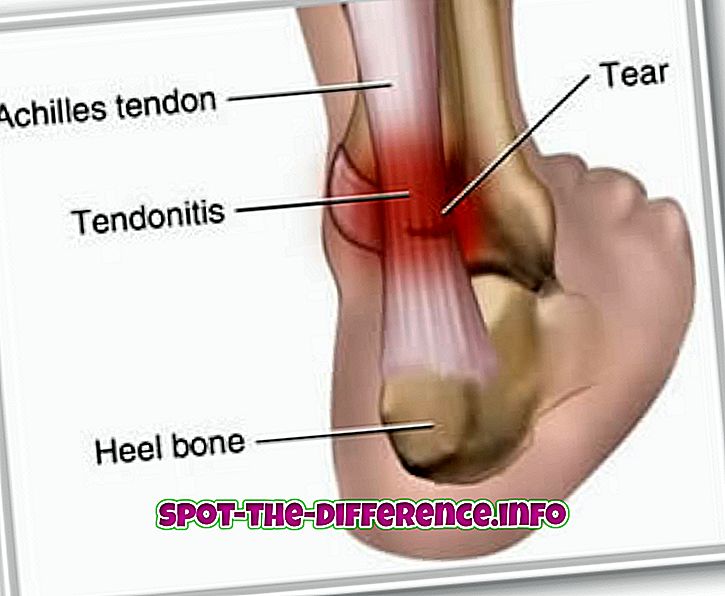
Oluline erinevus: Aatomite paigutus molekulis aitab määrata selle polaarsust. Molekul on polaarne, kui sellel on positiivne ja negatiivne laeng. Mittepolaarne molekul on vähem laenguga molekul.
Keemias tähendab polaarsus elektrilise dipooli või mitme pooluselise momendiga molekuli või selle keemilise rühma elektrilaengute eraldamist. Polaarsed molekulid toimivad molekulidevaheliste sidemete ja vesiniksidemete kaudu. Molekulaarne polaarsus sõltub molekulides olevate aatomite vahelise elektronegatiivsuse erinevusest. Polaarsus määrab ka mitmeid füüsikalisi omadusi, nagu pinna pinged, sulamis- ja keemispunktid ning lahustuvus.
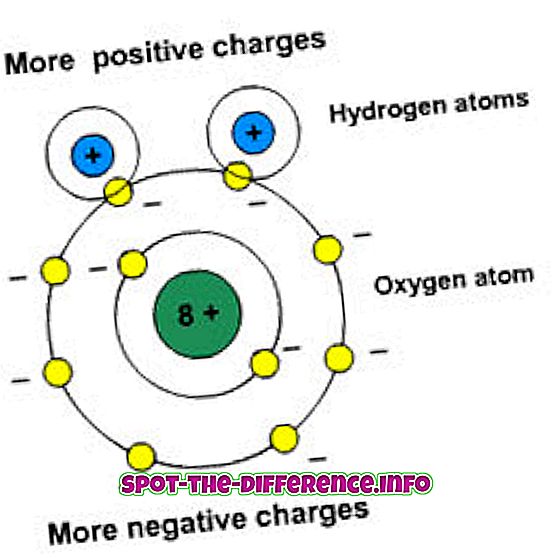
Polaarsus tähendab tasude eraldamist. Neil molekulidel on dipoolne moment. Dipoolmoment mõõdab sideme polaarsust. Polaarsed ained suhtlevad teiste polaarsete elementidega.

Mittepolaarsel molekulil ei ole piisavalt laengut. Mittepolaarsed molekulid jaotatakse sümmeetriliselt ja neil ei ole suurt hulka elektrilaenguid. Kui kahel aatomil või kahel samal aatomil on omavahel sama elektronsidem, tõmbuvad aatomid elektronpaari. See tõmbamine aitab neil jagada elektrone ja selline sidemete jagamine molekulide vahel on tuntud kui mittepolaarsed kovalentsed sidemed.
Polari ja mittepolaarse võrdlus:
Polar | Mittepolaarne | |
Määratlus | Polaarsetel ainetel on aatomil positiivne ja negatiivne laeng. | Mitte-polaarsetel ainetel ei ole aatomile suurt laengut. |
Liikumine | Neil on elektriline dipoolliikumine. | Neil ei ole dipooli liikumist. |
Tasu eraldamine | On laengute eraldamine. | Tasu eraldamine puudub. |
Koostoime | Nad suhtlevad teiste polaarsete ainetega. | Nad ei toimi koos teiste polaarsete ainetega. |
Näide | Vesi, alkohol ja väävel. | Õli. |