Oluline erinevus: aatomid on põhiosad, millest kõik on valmistatud. Aatomid on väikesed, vahemikus 0, 1 kuni 0, 5 nanomeetrit laiusega. Iga elemendi iga aatom koosneb prootonitest, neutronitest ja elektronidest. Molekulide valmistamiseks kogunevad erinevate elementide aatomid. See toimub keemilise reaktsiooni kaudu. Molekul on keemilise aine väikseim kogus, mis võib eksisteerida.
Element on puhas keemiline aine, millel on üks või üks aatomitüüp, mille aatomi number erineb. Aatomarv on tuletatud elemendi tuumas olevate prootonite arvust. Kokku on tuvastatud 118 elementi, mis on jagatud metalli, metalloidide ja mittemetallide vahel. Igal elemendil on oma omaduste kogum. Enamik elemente on saadaval maa peal, mõned neist on kunstlikult välja töötatud tuumareaktsioonide kaudu. Element on juba toorsaim ja seda ei saa enam jaotada. Kõik elemendid on toodud perioodilises tabelis, mis on loetletud aatomi numbriga.
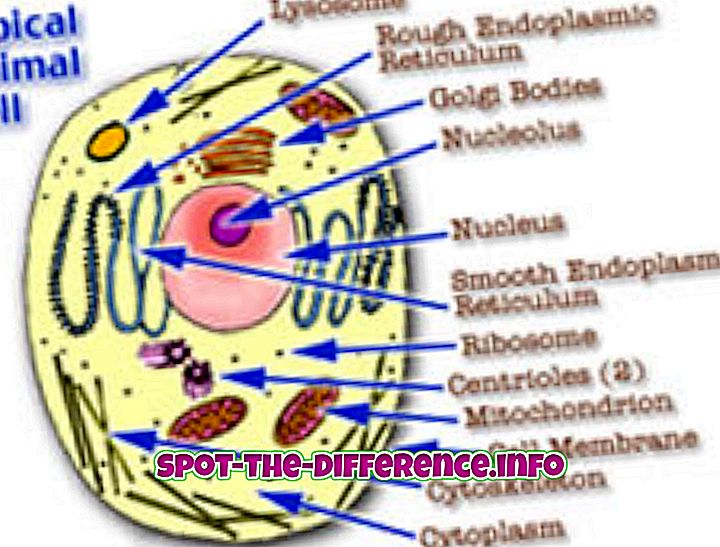
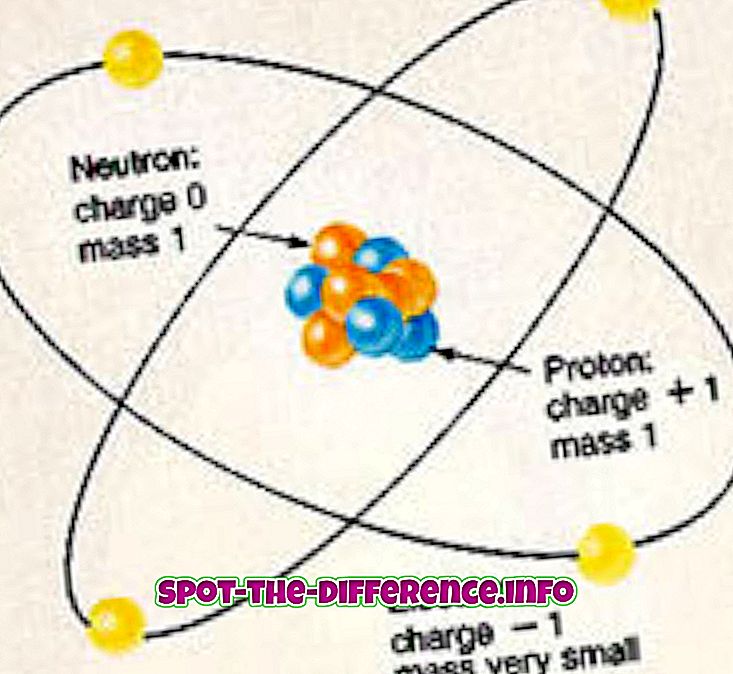
Iga elemendi iga aatom koosneb prootonitest, neutronitest ja elektronidest. Prootonid ja neutronid moodustavad aatomi tuuma ja asuvad aatomi keskel. Tuuma ümbritseb elektronide pilv, mis on elektromagnetilise jõuga seotud tuumaga. Elektronidel on negatiivne laeng, mis meelitab neid tuuma külge, kuna tuuma prootonitel on positiivne laeng. Neutronitel pole aga tasu.
Aatomites olevate prootonite, neutronite ja elektronide arv määrab selle elemendi. Näiteks: raua aatomil on 26 prootonit, 30 neutronit ja 26 elektroni. Igal raua aatomil on selline konfiguratsioon.
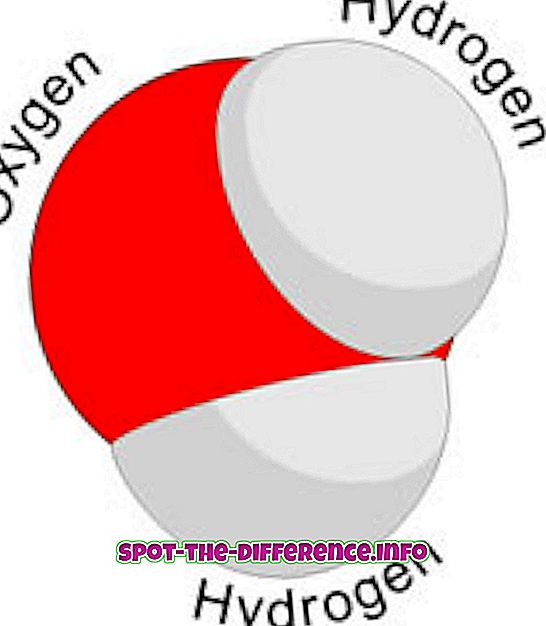
Molekulide valmistamiseks kogunevad erinevate elementide aatomid. See toimub keemilise reaktsiooni kaudu. Näiteks: kaks vesinikuaatomit ja üks hapnikuaatom ühendavad veemolekuli.

Molekul võib omada väga erinevaid omadusi elementidest, mis on valmistatud. Näiteks: vesi käitub väga erinevalt kui hapnik või vesinik, kuigi see koosneb kahest vesinikuaatomist ja ühest hapnikuaatomist.
Lisaks ei saa aatomi olemuselt looduses iseseisvalt olla, ilma et see oleks midagi seotud. Me ei leia kunagi ainult üht hapniku aatomit või ühte süsinikuaatomit. See on alati seotud millegi, näiteks O2 (hapnik) või CO2 (süsinikdioksiid). Molekuliga seotud molekul võib oma olemuselt olla iseseisvalt olemas, mistõttu leiame alati hapniku molekuli, süsinikdioksiidi molekuli, vee molekuli (H2O) jne.
Molekulis on aatomid kokku pandud teatud kuju või vormi. See sõltub peamiselt sellest, kui palju sidemeid aatom võib teha. Aatomid moodustavad molekule, moodustades üksteisega keemilisi sidemeid. Hapniku aatomitel on alati kaks sidet teiste aatomitega, süsinikuaatomitel on alati neli sidet teiste aatomitega ja lämmastikuaatomitel on alati kolm sidet teiste aatomitega. Sellepärast on teatud tüüpi molekulil alati konkreetne kuju, näiteks viisnurkne, kuusnurkne, külgmine, kahepoolne jne.
Molekulid kalduvad alati rühmitama, nende moodustumine sõltub nende olekust. Nagu näiteks gaasilises olekus, kipuvad molekulid lihtsalt lendama. Vedelas olekus kalduvad molekulid olema lõdvalt rühmitatud, et nad saaksid veel liikuda. Kui tahkes olekus on molekulid tihedalt kokku pakitud ja võivad ainult vibreerida.
Molekulid on tavaliselt esindatud molekulaarses valemis. Näiteks: O2, H2O, CO2, C6H12O6 (suhkur). Molekulaarne valem on elemendi nimi, millele järgneb selle elemendi aatomite arv molekulis.