Peamised erinevused: difusioon on protsess, mille käigus molekulid liiguvad ja liiguvad ühest kohast teise ilma lahtise liikumiseta. Efusioon on protsess, mille käigus molekulid liiguvad läbi tihvti suure kontsentratsiooni kohast madalasse kontsentratsiooni.
Mõisteid difusioon ja efusioon kasutatakse sageli paljudes teadustes, nagu keemia, füüsika ja bioloogia. Keemias on need kaks terminit gaaside kaks omadust. Need kaks on segadusttekitavad paljude inimeste jaoks, kes lihtsalt õpivad gaaside põhialuseid ja selle omadusi. Difusioon ja efusioon on kaks erinevat terminit, mis tähendavad kahte erinevat asja ja neid ei tohiks kasutada vaheldumisi. Difusioon tähendab gaaside võimet omavahel seguneda, samas kui efusioon viitab gaasi võimele liikuda läbi väikese tihvti. Difusiooni kasutatakse ka sotsioloogias, majanduses ja rahanduses, et viidata inimeste, ideede ja väärtuste levikule.
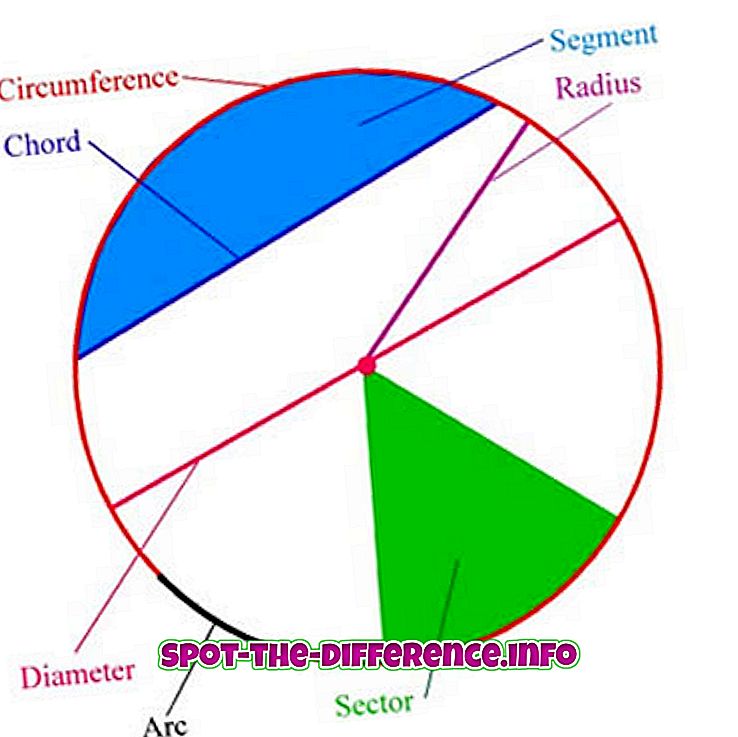
Difusioon on protsess, mille käigus molekulid liiguvad ja liiguvad ühest kohast teise ilma lahtise liikumiseta. Difusioon põhjustab molekulide liikumist või segunemist, kasutades ainult kineetilist energiat. Sõna „difusioon” on tuletatud ladinakeelsest sõnast „diffundere”, mis tähendab „levitada”. Difusioonis on molekulid pidevas liikumises ja kineetilise või termilise energia liikumisel kalduvad nad segunema teiste molekulidega, mille tulemuseks on lahutamatu segu. Võtame praktilise lähenemise, üks konteiner on jagatud A & B sektsioonidesse, kasutades tugevat partitsiooni; esimene osa täidetakse veega, teine osa on täidetud punase värviga. Nüüd, kui partitsioon on üles tõstetud, püüavad värvid ja vesi täita kogu konteineri. Seejärel värvib värvi aeglaselt veepunane, see on difusioon.
Difusioon põhjustab molekulide suurema kontsentratsioonipiirkonna ülemineku madalamale kontsentratsioonipiirkonnale, mille tulemuseks on kõigi molekulide segu. Difusioon peatub, kui kõik molekulid on ühtlaselt jaotunud. Difusioon ei piirdu veega ja toimib kõige paremini gaasilistes riikides, kus molekulidel on rohkem energiat ja võime segada teiste molekulidega. Difusioonile on kaks lähenemist: fenomenoloogiline ja atomistlik. Fenomenoloogilise lähenemise kohaselt liiguvad molekulid kõrgema kontsentratsiooniga piirkondadest madalama kontsentratsiooniga piirkondadesse. Aatomistliku lähenemise puhul peetakse difusiooni toimumist difundeeruvate osakeste juhusliku liikumise tõttu, kus difusiooni põhjustab soojusenergia, mis põhjustab nende segunemise. Difusioon mängib olulist rolli keha vajalike mineraalide, toitainete ja energia loomisel.

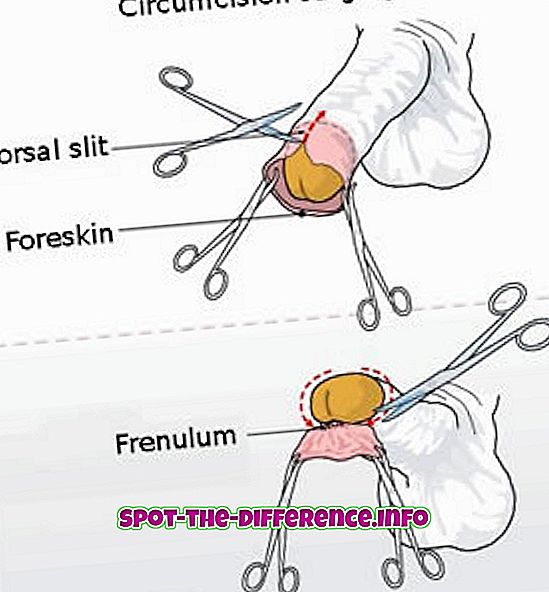
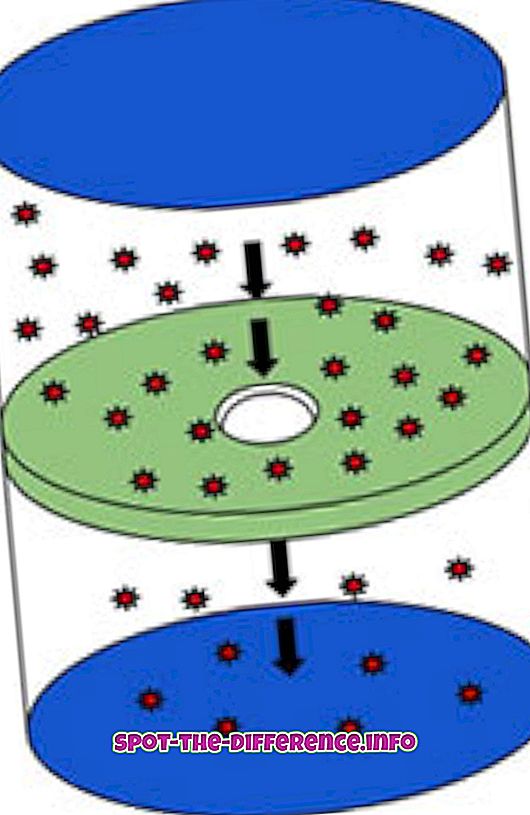
Efusioon on protsess, mille käigus molekulid liiguvad läbi tihvti suure kontsentratsiooni kohast madalasse kontsentratsiooni. Protsess kirjeldab gaasi võimet läbida väikest ava ilma molekulide kokkupõrgeteta. See juhtub siis, kui ava läbimõõt on oluliselt väiksem kui molekulide keskmine vaba tee. Keskmine vaba tee on liikuva osakesega läbitud keskmine kaugus järjestikuste kokkupõrgete vahel. Praktiline näide sellest on täita mahuti pudeliga suitsuga ja lasta pudelisse väike auk, suitsu, mis avaneb aukust välja, peetakse efusiooniks.
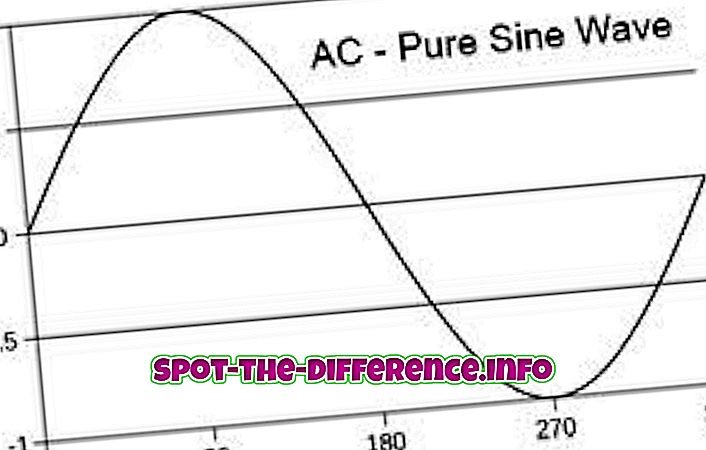
Šoti keemiku Thomas Graham sõnul on efusiooni mõõtmise valemi koostanud Graham'i seadus, mis määrab, kui kiiresti gaas liigub ja kuidas seda saab mõõta. Graham'i seaduse kohaselt sõltub gaaside eraldumise kiirus nende molekulmassist. Madalama molekulmassiga gaas väljub kiiremini kui kõrgema molekulmassiga gaas. Efusioon arvutatakse, mõõtes, kui palju molekule läbib augu sekundis. Sarnaselt on termodünaamikas gaasi efusioonikiirus pöördvõrdeline oma osakeste massi ruutjuurega.